글 목록
2024년 의약외품 정기감시 및 서면평가 가이드
2024년 의약외품 업체 대상 정기감시 도입
2024년도에는 의약외품 제조업체 및 수입업체를 대상으로 하는 정기감시가 계획되어 있습니다. 이는 각 지방 식약청에서 연간 계획에 따라 실시되며, 경인 식약청을 비롯한 여러 지방 식약청에서는 정기감시 대상 업체에게 이미 안내 공문을 발송한 상태입니다.
>> 서울지방식약청 기준 제출기한 4월 19일 금요일 까지
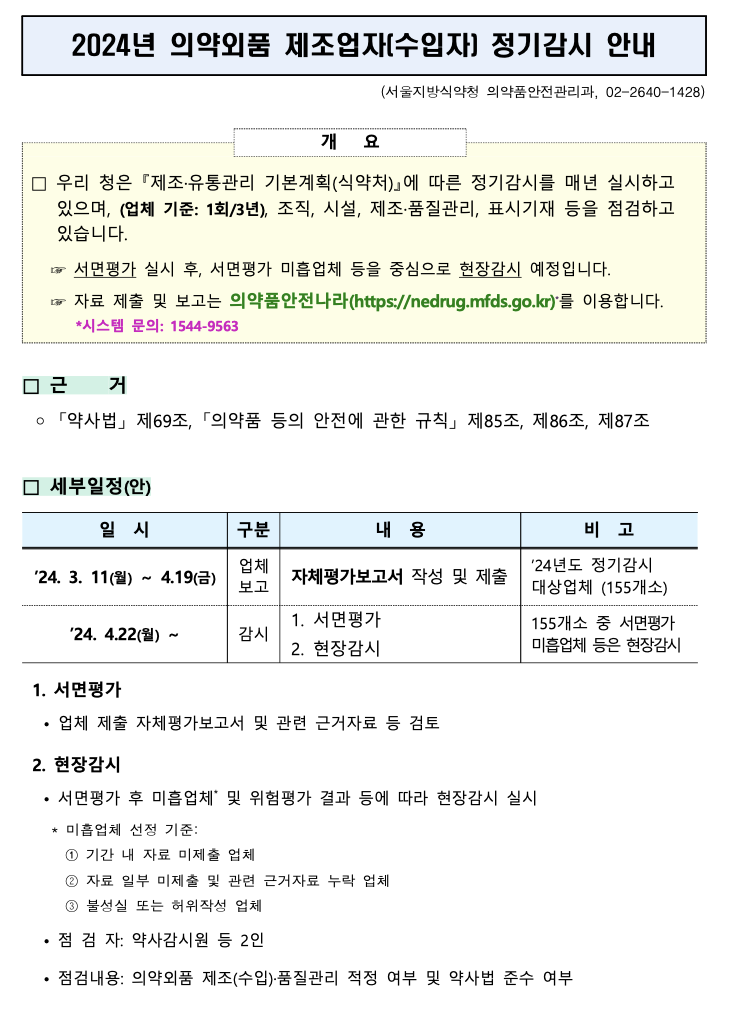

정기감시의 절차: 서면평가부터 현장평가까지
정기감시는 주로 두 단계로 진행됩니다. 첫 번째 단계는 서면평가로, 업체의 관리 상태를 점검하여 문제가 있는 업체를 선별합니다. 이후 문제가 있는 것으로 판단된 업체는 두 번째 단계인 현장평가를 받게 됩니다. 각 지방 식약청별로 세부 절차에 차이가 있을 수 있으며, 일부 지역에서는 잠재적 위험도 평가를 통해 현장점검 대상을 선정하기도 합니다.
- 서면평가
- 현장점검
서면평가의 중요성 및 제출 자료
서면평가에서는 업체가 자체적으로 관리 상태를 점검하고 필요한 자료를 제출합니다. 제출해야 하는 자료에는 제조소나 영업소에 필수적으로 갖추어야 하는 관리기준서, 기록서 등이 포함되며, 제조(수입)업자의 준수사항이 제대로 이행되고 있는지를 평가합니다. 특히, 제품에 대해서는 전년도 제조(수입)실적 상위 품목의 제조번호 3로트에 대해서만 제출하도록 하고 있어, 문서 관리의 중요성이 강조됩니다.


서면평가를 위한 제출 자료 상세 안내
제조업자를 위한 서면평가 제출 자료
- 제조업체 현황, 품목허가(신고) 현황
- 업체정보, 점검 품목명 및 제조번호
- 시설 및 환경관리, 제조관련기준 준수여부
- 제품 입출고 관리 및 품질관리
- 궐련형 금연보조제 제조업자의 준수사항
수입업자를 위한 서면평가 제출 자료
- 시설 및 환경관리 관련 자료
- 수입관리기준 준수여부 관련 자료
- 제품 입출고 관리 및 품질관리자료
관리의 중요성 및 전문가 활용의 권장
서면평가를 수월하게 통과하기 위해서는 평상시 문서 관리가 매우 중요합니다. 허가 후 관리는 매우 중요하며, 제조 및 품질관리 체계가 갖추어져 있지 않다면 즉시 업체 상황에 맞는 문서를 마련하고 체계적으로 관리할 필요가 있습니다. 또한, 전문 행정사의 컨설팅을 활용하는 것도 좋은 방법입니다.

결론
2024년 의약외품 업체 대상 정기감시는 업체의 자율적인 관리와 준비를 요구합니다. 정기감시를 성공적으로 통과하기 위해선 서면평가에 필요한 문서 관리와 준비가 중요하며, 필요시 전문가의 도움을 받는 것이 유익할 수 있습니다.


'식품의약품안전처 > 의약외품' 카테고리의 다른 글
| 의약외품 생리대 수입업 수임.처리 사례 및 절차 안내(제조 포함) (1) | 2024.05.01 |
|---|---|
| 의약외품 사용상의 주의사항 작성 민원인 안내서 (1) | 2024.05.01 |
| 의약외품 생리대 수입 절차와 주의사항 (0) | 2024.03.13 |
| 의약외품 광고 가이드라인(2023.5. 개정) (0) | 2023.06.05 |
| 의약외품 표시 가이드라인(2023.5. 개정) (0) | 2023.06.03 |





댓글