
복수의무인증제품의 인증 방법 및 국가통합인증마크 표시 요령
이 요령은 제품에 대한 인증, 검정, 등록, 인정, 심사, 검사, 신고, 형식 승인 등(이하 "인증"이라 한다)을 반드시 받도록 법령에 규정된 제품 중 2개 이상의 인증(이하 "복수 인증"이라 한다)을 받아야 하는 제품에 대한 인증 방법 및 국가통합인증마크(이하 "KC마크"라 한다) 표시 방법을 합리적으로 정함으로써 복수 인증에 따른 기업의 불편을 최소화하고 KC마크의 표시를 효과적으로 할 수 있도록 하는 것을 목적으로 하고 있습니다.
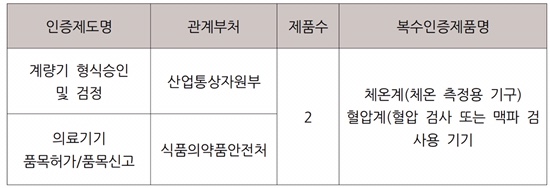
적용대상 및 복수의무인증 제품은 다음과 같습니다.
의료기기 품목 및 품목별 등급에 관한 규정
{의료기기법} 제3조 및 같은 법 시행규칙 제2조에 따른 의료기기의 품목 및 품목별 등급에 관하여 필요한 사항을 정함을 목적으로 한 규정입니다.
> 1등급 : 잠재적 위해성이 거의 없는 의료기기
> 2등급 : 잠재적 위해성이 낮은 의료기기
> 3등급 : 중증도의 잠재적 위해성을 가진 의료기기
> 4등급 : 고도의 위해성을 가진 의료기기
잠재적인 위해성에 대해 판단하는 기준은 아래와 같습니다.
1. 인체와 접촉하고 있는 기간
2. 침습의 정도(침습 : 질병발작의 시작이나 세균이 체내에 들어가 조직 내로 들어가는 것)
3. 약품이나 에너지를 환자에게 전달하는지 여부
4. 환자에게 생물학적 영향을 미치는지 여부
의료기기 기준 규격
{의료기기법} 제19조 규정에 따라 품질에 대한 기준이 필요하다고 인정하는 의료기기에 대하여 그 적용범위, 형상 또는 구조, 시험규격, 기재사항 등을 기준규격으로 정하여 의료기기의 품질관리에 적정을 기하는데 그 목적을 두고 있습니다.
적용범위는 {의료기기법} 제2조에 의하여 정의된 의료기기에 대하여 적용합니다.

의료기기의 전기.기계적 안전에 관한 공통 기준 규격
{의료기기법} 제19조 규정에 따라 품질에 대한 기준이 필요하다고 인정하는 의료기기에 대하여 그 적용범위, 시험규격 등을 기준규격으로 정하여 의료기기의 품질관리에 적정을 기하는데 목적이 있습니다.
적용되는 범위는 상기 의료기기 기준 규격과 동일합니다.
의료기기의 안정성 시험 기준
{의료기기법} 제6조 제5항, 제12조 제1항, 제15조 제6항 및 같은 법 시행규칙 제7조 제2항, 제15조 제1항에 따라 제출하는 의료기기 기술문서 심사자료와 의료기기 제조 및 품질관리 기준에 따른 의료기기의 안정성 시험에 관한 기준을 정함을 목적으로 합니다.
이외의 규정
> 의료기기 허가.신고.심사 등에 관한 규정
> 의료기기 제조 및 품질 관리 기준
> 의료기기의 전기.기계적 안전에 관한 고통 기준 규격
> 의료기기의 전자파 안전에 관한 공통 기준 규격
> 의료기기 생물학적 안전에 관한 공통 기준 규격
> 의료기기 안정성 시험 기준
> 의료기기 기술문서 심사기관 지정에 관한 규정
> 의료기기 부작용 보고 등 안전성 정보 관리에 관한 규정
> 의료기기 부작용 등 안전성 정보 관리에 관한 규정
> 의료기기 광고 사전 심의 규정
> 의료기기 재심사에 관한 규정
> 의료기기 재평가에 관한 규정
> 의료기기 임상시험 계획 승인에 관한 규정
> 의료기기 임상시험 기본 문서 관리에 관한 규정
> 의료기기 임상시험기관 지정에 관한 규정
> 추적관리대상 의료기기 지정
> 의료기기 표시.기재 등에 관한 규정
> 의료기기 허가.신고.심사 등에 관한 규정
> 추적관리대상 의료기기 기록과 자료 제출에 관한 규정
'식품의약품안전처 > 의료기기' 카테고리의 다른 글
| 복잡한 의료제품 인허가, 식약처와 사전상담 하세요 (0) | 2022.06.18 |
|---|---|
| 의료기기 제조업자 준수사항 (0) | 2019.12.25 |
| GMP 품질경영시스템의 이해 (0) | 2019.09.19 |
| 의료기기법 위반에 따른 행정처분 (0) | 2019.09.19 |
| 의료기기 기준규격의 지정 및 심사기관 업무 (0) | 2019.08.23 |


댓글